Tratamentos
O tratamento para a Amiloidose ATTR se desdobra em três aspectos: tratamento dos sintomas e sequelas, tratamento da doença propriamente dita e prevenção à transmissão da doença para os filhos.
Tratamento e acompanhamento dos sintomas e sequelas
Por ser uma doença multissistêmica, isto é, que atinge vários órgãos e sistemas, o acompanhamento e tratamento dos sintomas requer uma equipe multidisciplinar, que envolva neurologistas, gastroenterologistas, oftalmologistas, urologistas, nutricionistas, cardiologistas, nefrologistas, psicólogos, dermatologistas, ortopedista, fisiatras, entre outros, de preferência que tenham conhecimentos específicos sobre essa doença.
No acompanhamento são utilizados exames de condução nervosa (eletroneuromiografia) para monitorar a polineuropatia, assim como eletrocardiografia, ecocardiografia e holter para a cardiomiopatia, entre outros.
Exames de sangue constantes servem para monitorar o estado geral do paciente. Exames de função renal e oftalmológicos também são considerados.
Consulte aqui os centros de referência para diagnóstico, acompanhamento e tratamento da Amiloidose ATTR.
Tratamentos da Amiloidose ATTR
Atualmente existem 2 classes de tratamentos para a amiloidose ATTR. Os estabilizadores, que são pequenas moléculas que se ligam a proteína transtirretina e impedem a sua desestabilização, que é a causa da formação dos agregados de amilóide nos diversos tecidos do corpo humano. Já os inibidores da síntese da TTR são mecanismos que atuam no RNA das células do fígado, impedindo a produção da proteína ttr.
O diagnóstico precoce é de fundamental importância, pois os tratamentos não curam as lesões preexistentes.
ESTABILIZADORES
Tafamidis meglumina (20mg)
Nas últimas décadas, começaram a ser estudadas novas formas terapêuticas para a Amiloidose Hereditária, como a estabilização da TTR, inibição da produção da TTR, destruição das fibras amiloides insolúveis e inibição de sua agregação.
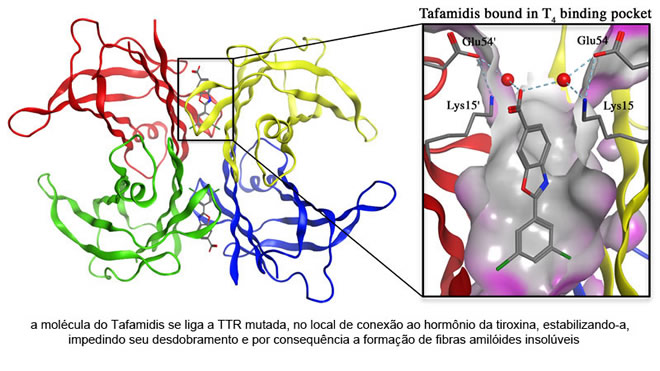
Desde a década de 90, o Dr. Jeffery W. Kelly estuda o mecanismo de como as proteínas se desagregam e formam fibras amilóides, e o que fazer para barrar esse processo. Kelly desenvolveu o medicamento Tafamidis, que age estabilizando a TTR anormal (mutada), evitando que se formem os depósitos de fibras amilóides e diminuindo assim a progressão da doença. Em 2006 recebeu o status de droga órfã pelo FDA e o EMA. O estudo com o medicamento foi conduzido em 2007 e seus resultados você pode acessar aqui.
Em novembro de 2011 a droga foi aprovada para comercialização pela Agência Europeia de Medicamentos (EMA) como o primeiro remédio para tratamento da Amiloidose Hereditária do mundo.
O medicamento é uma cápsula de uso oral, uma vez ao dia. É indicado para pacientes com Amiloidose Heditária ATTR não submetidos ao transplante de fígado com estágio 1 da polineuropatia.
Em novembro de 2016 obteve o seu registro no Brasil (Anvisa). Em janeiro de 2018 o CONITEC incorporou o Tafamidis à lista de medicamentos de alto custo do SUS e em outubro de 2018 foi publicado o Protocolo Clínico e Diretrizes Terapêuticas (PCDT) que indica como o deve ser realizado o diagnóstico, acompanhamento e tratamento dos pacientes e a distribuição do medicamento foi iniciada em outubro de 2019.
Tafamidis (61mg)
Um estudo de 30 meses para tratamento da cardiomiopatia amiloide hereditária e selvagem no New England Journal of Medicine com 2 dosagens do medicamento - 20mg e 80mg e foi comprovado que a dosagem maior (Tafamidis meglumina 80mg ou Tafamidis 61mg) obteve maior eficácia no tratamento da cardiomiopatia. Acesse aqui
O medicamento é uma cápsula de uso oral e deve ser tomada uma vez ao dia. 80mg de Tafamidis meglumina equivalem a 61mg de Tafamidis.
O Tafamidis 61mg foi aprovado para tratamento da amiloidose cardíaca selvagem e hereditária ATTR pela Anvisa em dezembro de 2019 e foi incorporado do SUS em 19 de junho de 2024, mas ainda não está disponível, pois o processo está em trâmites burocráticos.
Acoramidis
Acoramidis é uma molécula sintética desenvolvida para estabilizar a molécula da proteína TTR, a semelhança do Tafamidis, mas com alto poder de estabilização.
Trata-se de um comprimido que deve ser tomado de 12 em 12 horas.
Foi aprovado nos Estados Unidos em novembro de 2024 e na União Européia em fevereiro de 2025, para tratamento da amiloidose cardíaca ATTR (selvagem ou hereditária). Não há previsão de pedido de registro da Anvisa até o momento.
INIBIDORES
Inotersena (inotersena nonadecassódica)
O fármaco Inotersen é um oligonucleotídeo antisense desenvolvido para o tratamento da amiloidose hereditária por ATTR, para pacientes com quadro de polineuropatia. Ele atua interferindo no RNA mensageiro das células hepáticas, inibindo a produção da proteína transtirretina (TTR) que causa da doença. Clique aqui para ver o vídeo que explica o mecanismo de ação do medicamento.
O laboratório finalizou a fase III da pesquisa clínica multicêntrica internacional em meados de 2017. Os resultados da pesquisa foram divulgados no New England Journal of Medicine (acesse aqui) e o medicamento demonstrou ter alto potencial para tratar a doença, com perfil satisfatório de segurança, afim de retardar a progressão da doença e proporcionar mais qualidade de vida.
É uma injeção subcutânea onde o próprio paciente ou seu cuidador pode aplicar em casa, uma vez por semana. É obrigatório o acompanhamento do paciente para monitorização da função renal, hepática e das plaquetas quando tratado com Inotersen.
Foi aprovado no Brasil pela Anvisa em 29 de outubro de 2.019 para tratamento de pacientes adultos com Amiloidose Hereditária ATTR com polineuropatia nos estágios 1 e 2. É aprovado também nos EUA, Europa e Canadá.
Houveram 2 tentativas de incorporação do Inotersena ao SUS em fevereiro de 2022 e em dezembro de 2023 mas foram negadas pela Conitec, que alegou alto impacto orçamentário.
Patisirana (patisirana sódica)
O fármaco Patisiran é um RNA interference desenvolvido para o tratamento da amiloidose hereditária por ATTR (cardíaca ou neurológica). Ele atua interferindo no RNA mensageiro das células hepáticas, inibindo a produção da proteína transtirretina (TTR) que causa da doença. Clique aqui para ver o vídeo que explica o medicanismo de ação do medicamento.
O laboratório finalizou a fase III da pesquisa clínica APOLLO multicêntrica internacional em meados de 2017. Os resultados da pesquisa foram divulgados no New England Journal of Medicine (acesse aqui) e o medicamento demonstrou ter alto potencial para tratar a doença, com perfil satisfatório de segurança.
(Os Drs. Andrew Z. Fire e Craig C. Mello ganharam o Prêmio Nobel de Medicina em 2006 pela invenção desse método de silenciamento gênico.
É um medicamento administrado via infusão, uma vez a cada 21 dias, com uso de pré-medicação.
Foi aprovado pela Anvisa em 16 de fevereiro de 2020 para tratamento de pacientes adultos Amiloidose Hereditária ATTR com polineuropatia em estágios 1 e 2. É aprovado também nos Estados Unidos, Europa, Canadá, Japão e Suíça.
Em fevereiro de 2025 foi aprovado para tratamento da amiloidose cardíaca ATTR (selvagem e hereditária)
Houve uma tentativa de incorporação do medicamento no SUS em agosto de 2022 mas foi negada pela Conitec, que alegou alto impacto orçamentário.
Vutrisirana
A vutrisirana é a segunda geração da tecnologia de RNA interference desenvolvido para tratamento da amiloidose hereditária ATTR. Seu modo de ação é igual ao da Patisirana.
Sua formulação avançada permitiu ser desenvolvido para aplicação subcutânea em longos intervalos de tempo, dando mais autonomia ao paciente, além de eliminar a necessidade da pré medicação.
Trata-se de uma injeção subcutânea aplicada a cada 3 meses e está aprovado em diversos países. No Brasil, ela foi aprovada pela Anvisa em dezembro de 2022 para tratamento da amiloidose hereditária ATTR com polineuropatia.
E em abril de 2025, a Anvisa aprovou a ampliação da indicação da vutrisirana para tratamento também da amiloidose por transtirretina com cardiomiopatia (ATTR-CM) – tanto na forma selvagem (wtATTR) quanto hereditária (hATTR).
O medicamento, que já era indicado para hATTR com polineuropatia, passa a ser também uma opção importante para pacientes com acometimento cardíaco.
Houve uma tentativa de incorporação ao SUS em junho de 2024 mas foi negada pela Conitec, que alegou alto impacto orçamentário.
Eplontersena
É a segunda geração da inotersena, onde foi aprimorada a molécula, permitindo assim uma dosagem bem menor e em consequência a diminuição drástica dos efeitos colaterais.
Como a inotersena, é uma injeção subcutânea, entretanto o período entre as aplicações é de 1 mês e não necessita de monitoramento a cada 2 semanas.
Foi aprovada nos Estados Unidos em dezembro de 2023 e na União Europeia em outubro de 2024 para tratamento da Amiloidose hereditária com polineuropatia e também no Brasil pela Anvisa (Resolução-RE nº 3.777, de 25 de setembro de 2025).
Estudos para tratamento da amiloidose cardíaca (hereditária e selvagem) estão sendo conduzidos. « Voltar